检查员总结!制药用水系统检验26个常见缺陷及注意事项
检查员总结的26个常见缺陷
饮用水没有进行监测或取水点选择不合理,不具有代表性。
用于水系统监控的电导率、TOC分析仪等设备没有定期校准记录。
制水间测定pH值用的缓冲液标签上的名称未按《中国药典》(2020年版)规定标准名称进行标识。
水系统日常运行控制参数数据,超出了系统验证时的控制参数范围。
水系统在完成维修、改造后,没有根据实际情况及时对水质情况进行分析确认。
日常监测取样点设计不合理,如:取样点数量不够、布局不符合要求、取样点不易取样等。
纯化水系统采用饮用水+预处理系统+一级RO的配置方式,未能确保产水质量达到纯化水的标准。
纯化水储罐呼吸器未设置过滤器。
使用点U型弯较长,有超过管径6倍的死水盲管。
水系统储罐、管道选材所用材质查无档案。
水系统管道使用的304L不锈钢材质,未实施酸洗钝化。
制水间有蜘蛛网,地面有积水。
纯化水的分配系统无臭氧等消毒设施。
纯化水储存未开启循环或无循环。
未对原水进行定期监测和记录。
未按规程对纯化进行定期监测。
未建立纯化水微生物限度检测的警戒线和纠偏限。
水系统年度质量回顾分析报告未对微生物情况进行趋势分析。
操作人员不熟悉水系统清洗消毒周期和操作方式。
未设置警戒限度和纠偏限度,无纠偏记录。
操作规程中未明确规定纯化水微生物污染达到警戒限度和纠偏限度后,如何进行处理的内容。
水系统日常监测过程中,发现微生物超过纠偏限时,未按规定进行偏差分析和采取纠正预防措施。
水系统的设计与运行不符合规定,如:
(1)纯化水某段管路的坡度为0.31%,不符合《洁净室施工及验收规范》规定的应不小于0.5%坡度要求。
(2)注射用水系统回水流量小于1m3/h。 (3)注射用水系统停止运行超过1个月,储罐未排空。 纯化水和注射用水微生物限度检测未及时记录结果,但检测样品已销毁。
未使用纯化水作为注射用水系统和纯蒸汽发生器的源水。
注射剂用容器和内包装材料,其最终淋洗的注射用水未检验内毒素,而这些容器和内包装材料不再进行热原处理。
<制药用水理化检测脑图>
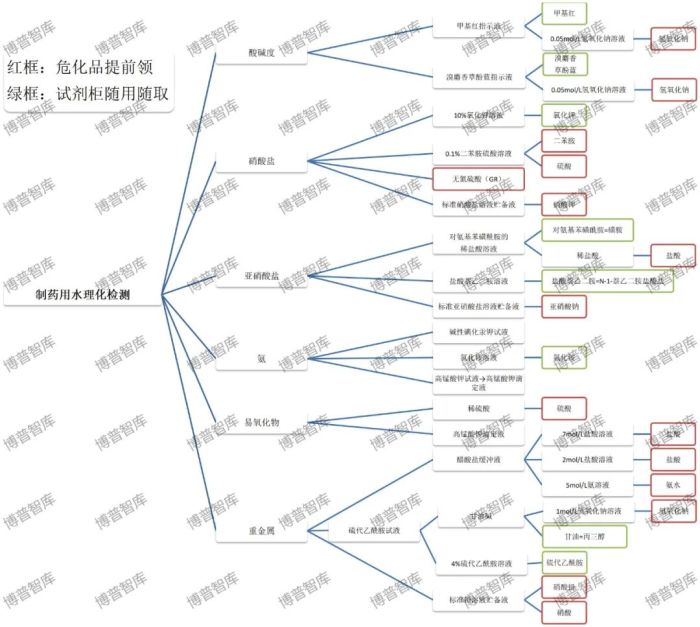
检纯化水微生物限度检查注意事项
过程分析技术(PAT)在提出至今已深入制药行业的方方面面。过程控制的引入和提升不但大大节省了人力,提高生产效率;更重要的是,通过PAT可以大大降低生产制造风险,对异常情况可以做出更快速的响应,将危害和损失降到最低。
GMP质量圈
展源
何发
相关文章
-

制药用水的类型
2021-05-26
-

制药用水的TOC分析
2020-05-27
-

制药用水纯化技术专题
2021-05-24
-

制药用水的TOC分析技术
2020-05-27
-

制药用水单元操作有关问题
2021-05-28
-

制药用水8大注意事项!
2024-04-30
-

新版GMP对制药用水的要求
2021-05-31
-

GMP制药用水详解(新版)
2021-05-11
-

中国药典(GMP)制药用水要求详解
2020-05-27

加载更多