浅谈ADC药物脱靶毒性及改进策略
当下的ADC赛道异常火热,仅在过去的三年中,美国食品和药物管理局(FDA)批准的ADC数量增加了两倍。抗体药物偶联物(ADC)作为一类快速发展的抗癌药物,目前临床使用的药物有12种。
尽管最近取得了巨大成功,但由于潜在的脱靶毒性和不利的风险-收益分析,许多ADC药物在临床开发过程中面临着失败的困境。即使是那些已被批准用于临床的ADC,由于无法接受ADC相关的毒性,也会导致相当一部分接受治疗的患者需要减少剂量、推迟治疗,甚至停止治疗。
1
ADC药物背后的阴霾:毒性
抗体药物偶联物(ADC)是一种近年来快速发展的抗癌治疗药物,有100多种ADC正在进行临床研究。目前,美国食品和药物管理局(FDA)批准了12种ADC。
ADC由单克隆抗体(mAb)通过化学连接物与细胞毒性小分子药物(即有效载荷)连接而成。在过去的数十年间,尽管ADC取得了一定的成功,但由于存在严重的毒性问题,ADC的临床开发一直与高失败率有关(图1)。
因此,需要将可耐受ADC剂量限制在具有实质性抗癌功效所需的水平以下。并且,即使是已获得FDA批准的ADC,也有相当一部分患者需要支持性治疗以减轻ADC相关毒性的严重程度,许多患者需要减少剂量、延迟治疗或停止治疗。先前ADC的开发经验表明,ADC的临床毒性主要与有效载荷成分有关。



图1.已批准ADC药物的常见不良反应
2
ADC药物产生毒性的机制
据估计,只有大约0.1%的ADC注射剂量被传递到靶向病变细胞群,绝大多数给药剂量靶向健康细胞内进行分解,这可能导致不必要的“off-site” 毒性。ADC的“off-site” 毒性可分为“on-target”或“off-target”,其中,“on-target”脱靶毒性通过ADC与健康细胞上的靶细胞表面蛋白结合进行。研究表明,ADC的每个组成部分,包括抗体、连接子和有效载荷,都可能影响ADC诱导毒性的程度。ADC对正常细胞的毒性主要通过靶点依赖性和非靶点依赖性机制发生。

图2. ADC毒性机制
2.1靶点非依赖毒性
迄今为止,大多数ADC的 “off-site”毒性与细胞毒性载荷的脱靶递送有关,脱靶载荷递送是ADC耐受性的关键驱动因素,并最终影响患者使用的推荐剂量。一般来说,导致严重毒性的药物可能会在临床前开发的早期阶段迅速被发现,从而在推进到临床研究之前终止。
靶点非依赖毒性分为ADC有效载荷递送脱靶及脱靶受体介导的ADC摄取。ADC有效载荷递送脱靶主要是由于连接子-载药不稳定导致循环中载药过早释放导致。脱靶受体介导的ADC摄取是指FcγRs、甘露糖受体(MR)结合和受体介导的内化介导ADC脱靶造成的毒性。
2.2 正常细胞非特异性内吞造成的毒性
尽管有证据表明有效载荷介导的脱靶机制是大多数ADC毒性的关键因素,但也有研究发现ADC与健康组织中表达的靶抗原的结合也可能导致显著的毒性。例如,在临床试验中,约40%的患者使用维汀-恩弗妥单抗治疗的患者出现异常,这被认为是一种靶向毒性,因为ADC靶点(nectin-4)在唾液腺中也有表达。正常细胞可以通过受体依赖性和非受体依赖性(非特异性内吞)机制摄取/转运完整的ADC药物。
3
常见的ADC相关剂量限制毒性
3.1嗜中性白血球减少症
中性粒细胞占粒细胞的40% - 70%,是先天性免疫系统的重要组成部分。严重中性粒细胞减少症是一种常见的剂量限制性毒性,与大多数利用缬氨酸-瓜氨酸可切割连接剂的MMAE - ADC相关,包括维布妥昔单抗、泊洛妥珠单抗、维汀-恩弗妥单抗和维汀-替索妥单抗等。此外,在使用具有可切割连接剂的其他有效载荷的ADC中,也常报告≥3级中性粒细胞减少症,如卡奇霉素、SN-38、、PBD、DM4和多西环素等。中性粒细胞减少症在使用稳定连接剂治疗的ADC患者中较少见,如:BLENREP®或恩美曲妥珠单抗。
ADC相关的中性粒细胞减少症似乎与释放有效载荷的累积血浆暴露相关(例如,过早释放后或从ADC分解代谢的细胞内位点分布后)。除了上述脱靶机制外,靶点依赖机制也可能导致靶向白血病抗原的ADC的中性粒细胞减少。
3.2血小板减少症
血小板减少症是一种常见的脱靶毒性,与使用稳定连接剂(SMCC-DM1或MC-MMAF)的ADC有关,也与使用DNA交联剂卡奇霉素有关。例如,99%的急性髓系白血病患者发生≥3级血小板减少,42%的急性淋巴细胞白血病患者接受吉妥珠单抗治疗。在接受恩美曲妥珠单抗治疗的乳腺癌患者中,有14.5%的患者报告了≥3级血小板减少,在接受BLENREP®治疗的多发性骨髓瘤患者中,有21%的患者报告了≥3级血小板减少。
然而,血小板减少症的确切机制仍不清楚。ADC在巨核细胞分化过程中通过fcγr介导的或小胞饮途径的非特异性摄取被认为是一个可能的原因。然而,根据观察,ADC相关血小板减少的临床表现通常发生在24小时内,明显短于典型的血小板寿命8 - 10天,可能有其他因素导致血小板减少。
3.3周围神经病变
周围神经病变的临床表现包括感觉相关症状,如四肢麻木、刺痛和疼痛,或在较小程度上有运动相关症状,如肌肉无力。周围神经病变是一种常见的不良反应与小管蛋白抑制化疗药物,如紫杉烷和长春花生物碱。同样,外周神经病变是一种重要的剂量限制性脱靶毒性,与使用微管蛋白抑制剂有效载荷结合可切割连接剂(如vc-MMAE、SPP-DM1和SPDB-DM4)的ADC有关。因此,微管蛋白抑制载荷对微管的破坏可能导致周围神经病变。
3.4 眼毒性
眼毒性是含有SPDB-DM4连接剂载荷的ADC的关键脱靶剂量限制毒性之一,如雷坎妥组单抗、索星-米妥昔单抗和雷星-考妥昔单抗,或mc-MMAF连接剂载荷,如BLENREP、AGS-16C3F和SGN-75。眼睛对ADC细胞毒性的易感性可能是由于几个因素,包括充足的血液供应,快速分裂的上皮细胞群的存在,以及几种细胞表面受体的高表达。在临床情况下,ADC相关的眼部不良事件包括视力模糊、角膜炎、干眼和微囊性上皮损伤。然而,与ADC相关的眼毒性机制仍然知之甚少。一项研究证实完整的ADC通过大胞饮的非特异性摄取是ADC脱靶眼毒性的机制。然而,也有研究表明靶点介导的ADC摄取也可能导致眼毒性的产生。

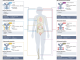
图3.常见的ADC相关剂量限制毒性
4
降低ADC药物毒性的策略
研究表明,强效的ADC通常会导致更高的疗效,但也会导致危及生命的毒性的发生率增加,导致临床应用受到限制。目前,ADC领域的研究焦点正在转向通过减轻ADC毒性来拓宽治疗窗口的策略,因为这种策略可能会增加最大耐受剂量MTDs并改善临床结果。
4.1优化修饰ADC的连接链及有效载荷
传统的ADC连接技术主要采用赖氨酸的氨基残基或半胱氨酸的巯基残基的非特异性连接,这会导致DAR和疏水性的相当大的异质性,DAR值从2高至6。研究表明,高负载ADC通常在血浆中不稳定,在肝脏中表现出较高的非特异性摄取率,导致脱靶毒性增加。
目前,研究人员已经开发了可以精确地将指定数量的细胞毒有效载荷结合在定义抗体位置的策略。这些技术将实现更精确的DAR控制,并由于其共轭到更稳定的位置,从而提高共轭载荷的稳定性,同时还简化了ADC制备工艺和设计。
研究发现,通过对连接子的修饰可以降低ADC的疏水性,降低毒性。目前基于连接链的修饰策略包括:PEG修饰、引入基于自消除链形式的连接链、引入抗非特异性肽酶裂解稳定性的连接剂等。此外,有效载荷化学结构的修改也可能改善ADC耐受性。
4.2抗体的修饰
由于ADC的大多数靶点在健康组织中也有一定程度的表达,因此通过ADC结合在这些组织中传递细胞毒性载荷可导致“off-site“毒性产生。为了降低靶向毒性,研究人员已经开发了基于抗体药物偶联物的前药形式(PDC),其中抗体的结合区域被抗独特型肽所掩蔽,这些肽通过蛋白酶敏感肽连接物连接到抗体。其目的是通过肿瘤微环境中的优先激活来增强肿瘤的选择性,其中肿瘤微环境高表达的蛋白酶活性会切割掩蔽肽,从而使PDC与靶抗原结合。掩蔽肽的缓慢切割降低了PDC与健康细胞中靶抗原的结合程度,并降低了毒性,增强ADC的肿瘤内分布、疗效和治疗指数。
另一种降低靶向毒性的方法是通过开发针对两种肿瘤相关抗原的双特异性抗体。这种方法增强了选择性,因为只有在两种抗原高度共表达的细胞上才能观察到ADC的强烈结合。
4.3优化用药方案
分次给药的临床用药方案已被证明可以改善ADC的治疗指数。例如,Mylotarg最初于2001年被批准用于治疗CD33阳性AML,剂量为9mg /m2,至少间隔两周。然而,观察到很高的严重的临床毒性发生率,包括血小板减少症(99%),中性粒细胞减少症(97%),≥3级高胆红素血症(23%),≥3级丙氨酸转氨酶或天冬氨酸转氨酶水平升高,而与护理标准相比,疗效没有明显改善。因此,Mylotarg于2010年退出市场。
最近,ADC的分次给药的策略被引入,这样患者在给药周期的第1天、第4天和第7天接受3次3mg /m2的9 mg/m2剂量,从而获得可接受的毒性分布。Mylotarg的PK/PD分析表明,其毒性由峰值血浆浓度驱动,而其疗效由暴露量驱动。因此,在维持药物暴露水平的同时,分段给药可降低峰值血药浓度,降低毒性。经过修改的给药方案,Mylotarg于2017年重新获批临床使用。
4.4 逆靶向策略
一项研究表明,采用有效载荷结合抗体的“反向靶向”策略,可以提高ADC的治疗选择性。简而言之,有效载荷结合抗体片段(又名有效载荷结合选择性增强剂或PBSE)与ADC共同使用,以实现从血浆中结合、中和和清除释放的有效载荷,减少与ADC毒性相关的组织中释放有效载荷的暴露。
目前,抗体片段已被广泛用于减轻药物和毒素的不良反应,包括使用抗药物抗体来增强区域化疗的药代动力学选择性。PBSE技术可能在减轻由释放有效载荷介导的许多“off -site”毒性方面具有实用价值,有可能大大提高ADC的安全性和有效性。
5
小结
抗体-药物偶联物ADC是基于癌细胞与健康细胞表面抗原的差异表达的新型抗癌药物,其目的是增加抗癌药物递送的选择性,并拓宽传统化疗的治疗窗口。然而,ADC的临床应用会受到剂量限制的毒性的影响。目前,大量的研究工作已经投入到了解ADC介导的毒性机制,并制定相应策略来提高ADC的耐受性,从而提高疗效。我们相信,未来的ADC药物一定可以一扫阴霾,大放异彩!
参考文献
1、Mechanisms of ADC T oxicity and Strategies to Increase ADC T olerability. https://doi.org/10.3390/cancers15030713
2、Antibody–drug conjugates for cancer. Lancet 2019, 394, 793–804.
3、A Brief Introduction to Antibody–Drug Conjugates for Toxicologic Pathologists. T oxicol. Pathol. 2018, 46, 746–752.
4、Antibody–drug conjugates as novel anti-cancer chemotherapeutics. Biosci. Rep. 2015, 35, e00225
5、Effects of antibody , drug and linker on the preclinical and clinical toxicities of antibody-drug conjugates. MAbs 2016,8, 659–671.
药渡
展源
何发
相关文章
-

ADC药物质量专题
2023-11-06
-

ADC药物的研发策略与挑战
2022-07-13
-

ADC药物管线成功的关键指标
2023-02-06
-

QC, IQC, IPQC, QA,到底是什么鬼?
2020-05-27
-

AAS法分析茶叶中的铅,镉,砷
2020-05-27
-

ADC未来之路
2023-06-28
-
ADC的毒性来自哪里?
2023-08-04
-

二维液相色谱与高分辨质谱联用表征分析抗体偶联药物(ADC)
2023-06-08
-

HPLC检测器,你了解吗?
2024-03-06

加载更多