HILIC 色谱柱的使用注意事项
想要搞懂Hilic色谱柱,首先要明白Hilic的流动相和固定相。
1、流动相
在大多数的Hilic分离中,采用的流动相为含有少量水/缓冲液与有机相混合(典型的是乙腈),水的比例为3%-40%之间。
水的比例不低于3%是由于Hilic色谱的保留机理决定的,普遍认为Hilic色谱流动相中的水会被吸附到极性固定相的表面形成水膜,然后分析物在水膜和流动相之间进行液液分配作用,加上极性官能团和固定相之间的氢键作用力,离子官能团之间的静电作用力等,实现被分析物的保留。水膜的作用非常重要,所以Hilic流动相中至少含有3%的水。当水的比例大于40%时,保留一般很弱(k≈0)。
2、固定相
应用于Hilic色谱的固定相有:纯硅胶柱、氨基柱、二醇基柱、酰胺基柱等。纯硅胶柱有固定相不易流失的优点,在使用CAD、ELSD和LC-MS检测器时,最受欢迎;氨基柱,在Hilic色谱中的应用,特别适合碳水化合物(糖类)分离;二醇基柱,亲水性很好,可以提供不同的选择性。
Hilic和正相色谱相比
1、固定相的区别
同样是Silica,NH2,Diol柱,与用于正相色谱中的色谱柱不同,专为Hilic色谱设计的色谱柱,可以用于水/有机物的流动相中,换句话说,Hilic色谱对固定相的耐水性要求更高,否则会因固定相的水解,出现基线噪音大、色谱柱寿命短等问题。所以用于正相色谱中的色谱柱,不一定能用于Hilic色谱。而适用于Hilic色谱的色谱柱,可以用于正相色谱中。
2、应用范围的差异
正相色谱主要用于极性大的脂溶性化合物,而Hilic色谱主要用于极性大的水溶性化合物。
3、总结
和正相色谱相比,用于Hilic色谱中的Silica/NH2/Diol等色谱柱耐水性更好,Athena NH2-RP在Hilic色谱糖类分析中表现优异。
对于极性强的化合物,如果在正己烷、异丙醇中溶解度较好,推荐用正相色谱,如果在水中溶解度较好,推荐用Hilic色谱。
Hilic和反相色谱相比
1、保留行为差异
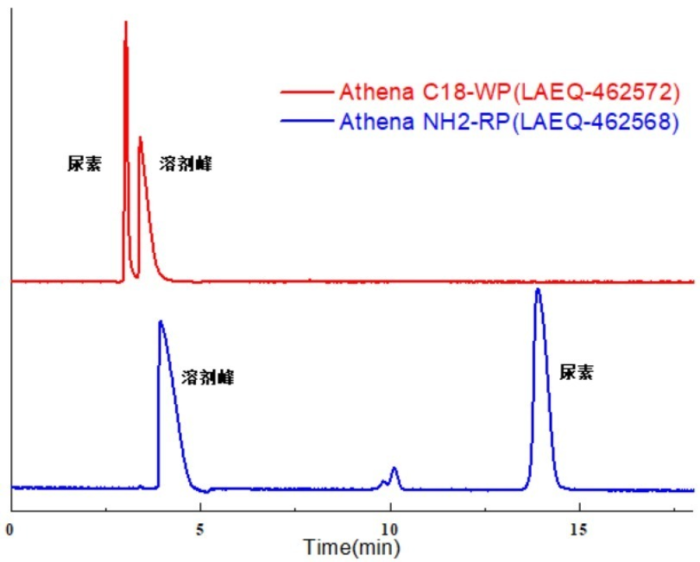
和反相色谱相比,Hilic色谱对极性大的水溶性化合物保留能力更强。极性较强的尿素,在Athena C18-WP (LAEQ-462572)没有保留,而在Athena NH2-RP (LAEQ-462568)可以很好的保留。
2、流动相中水的洗脱强度
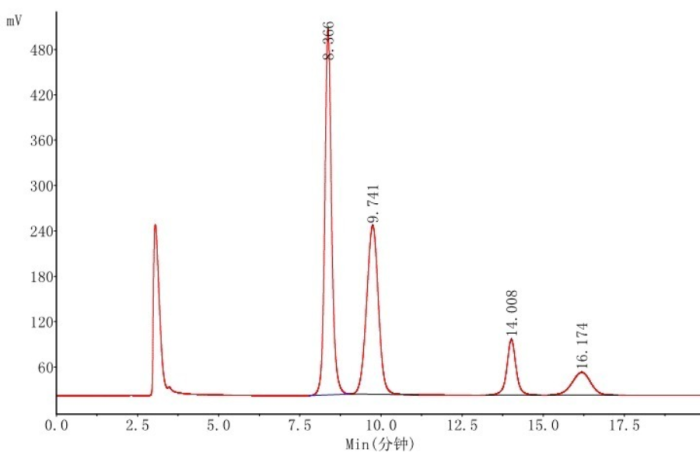
以Athena NH2-RP 4.6 × 250mm,5μm (LAEQ-462568)对糖类物质的分析为例。
流动相:乙腈/水(75:25)
色谱峰:1.果糖 2.葡萄糖 3.蔗糖 4.麦芽糖
应用:蜂蜜 中国药典2020年版一部 P374
流动相:乙腈/水(70:30)
色谱峰:1.蔗糖 2.乳糖
应用:乳糖 中国药典2020年版四部 P690
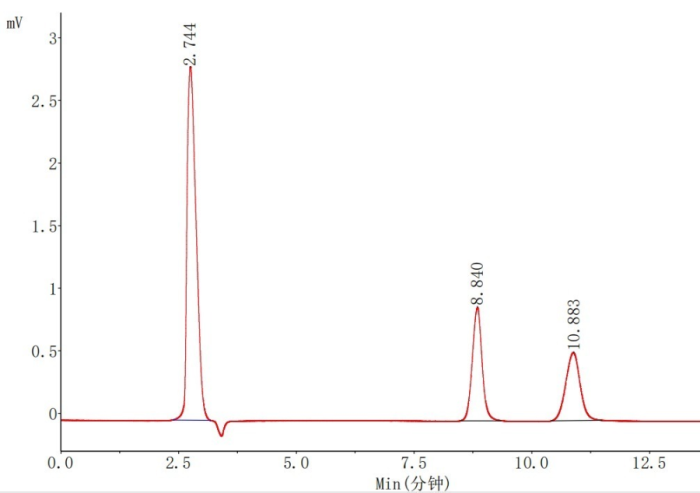
对比蜂蜜和乳糖应用,采用同一支Athena NH2-RP 4.6 × 250mm,5μm (LAEQ-462568)色谱柱,流动相从乙腈/水(75:25)变为乙腈/水(70:30)后,蔗糖的出峰时间从14.008min缩短至8.840min,流动相中水相比例增加,目标化合物出峰变早。我们知道,反相色谱中,流动相中水相比例增加,目标化合物的出峰会变晚。在Hilic色谱中,流动相中的水相部分表现为强溶剂,这和传统的反相色谱完全相反。
3、总结
对于极性大的亲水性化合物,在反相色谱中很难保留,可以用Hilic色谱增加保留。
在反相色谱中,流动相中的水相部分表现为弱溶剂,而在Hilic色谱中,水表现为强溶剂。
表1 反相、正相、Hilic色谱对比
Hilic色谱作为正相和反相色谱的补充,采用极性的固定相和流动相,在分析极性强的水溶性化合物中有很大优势。
通常情况,流动相中水相比例为3%-40%,水相比例太高,一方面目标化合物保留太弱,另一方面加快键合相的水解。
固定相的耐水解性要求更高,如Athena NH2-RP在Hilic色谱中特别适合糖类物质的分析,基线噪音小,色谱柱寿命长。
HILIC 色谱柱的使用注意事项
1、HILIC 色谱柱的平衡
使用 50 倍柱体积的 50/50 的乙腈/水相缓冲溶液(缓冲液的最终浓度为 10mM)平衡新色谱柱。
在开始进样前,用 20 倍柱体积的起始流动相平衡色谱柱。
进行梯度分析时,进样间隔需要用 10 倍柱体积起始流动相平衡色谱柱,色谱柱平衡不充分将导致保留时间漂移。
-
流动相中总是至少保持 5%的极性溶剂(如 5%水相缓冲液,5%甲醇或 3%甲醇+2%水相缓冲液等),保证 HILIC 硅胶填料始终被水浸润。 -
在流动相或梯度中至少保持有机溶剂(如乙腈)的比例不低于 40%。 -
不要使用磷酸盐缓冲溶液体系,因为磷酸盐缓冲液在 HILIC 色谱模式下会析出;使用磷酸则没有问题。 -
甲酸铵或乙酸铵水溶液缓冲系统比甲酸或乙酸的水溶液重现性更好。如果不能使用缓冲液而一定要使用流动相添加剂如甲酸,最好使用 0.2%的浓度而非 0.1%。 -
为得到最好的峰形,在流动相或梯度中总是保持缓冲系统的浓度为 10mM。
-
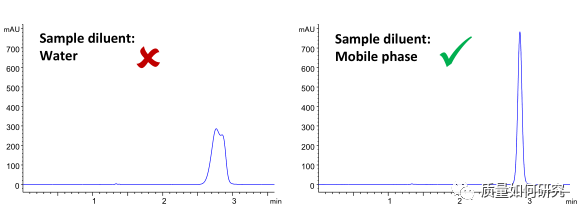
如果可能,尽量用 100%乙腈溶解样品进样。避免使用水配制样品溶液,请选择较弱的 HILIC 溶剂,如乙腈、甲醇、异丙醇等配制样品溶液。 -
最常用的稀释剂为 75/25 乙腈/甲醇,这个体系充分平衡了样品的溶解度和峰形两个因素。 -
不要用水或 DMSO 做稀释剂,它们将导致峰形变得很差。 -
使用反相 SPE 技术将水或 DMSO 置换成乙腈再进样。如果不能这样操作,用有机溶剂稀释水或 DMSO。
-
开始时可以运行一个 95%乙腈至 50%乙腈的梯度,如果样品不保留,使用 95/3/2的乙腈/甲醇/水相缓冲溶液的流动相进行等度分析。 -
将流动相中的水换成甲醇、丙酮或异丙醇也可以增加极性化合物的保留。 -
请确保洗针溶剂/冲洗溶剂包含和流动相一样的高比例有机相,否则峰形会受到影响。
-
用 50/50 的乙腈/水清洗以去除极性污染物。如果清洗无效,可用 5:95 的乙腈/水清洗色谱柱。 -
如果系统压力上升至超过设定的压力限或者突然出现色谱峰分叉,通常是需要更换保护柱的信号。
展源
何发
相关文章
-

选对色谱柱,快速开发方法
2020-05-27
-

填料对HILIC色谱柱性能有哪些影响?
2023-05-09
-
填料对HILIC色谱柱性能有哪些影响?
2023-09-25
-

色谱峰裂分,前拖尾的诊断
2020-05-27
-
检测有机氯类农药,气相色谱法检测法
2021-01-12
-

QC, IQC, IPQC, QA,到底是什么鬼?
2020-05-27
-

AAS法分析茶叶中的铅,镉,砷
2020-05-27
-

RRHD色谱柱
2020-05-27
-

HPLC系统色谱峰扩展与色谱柱柱效
2023-08-02

加载更多